Clinical study on the expression of CD56 in newly diagnosed multiple myeloma patients and the efficacy of induction therapy based on bortezomib combined with lenalidomide
-
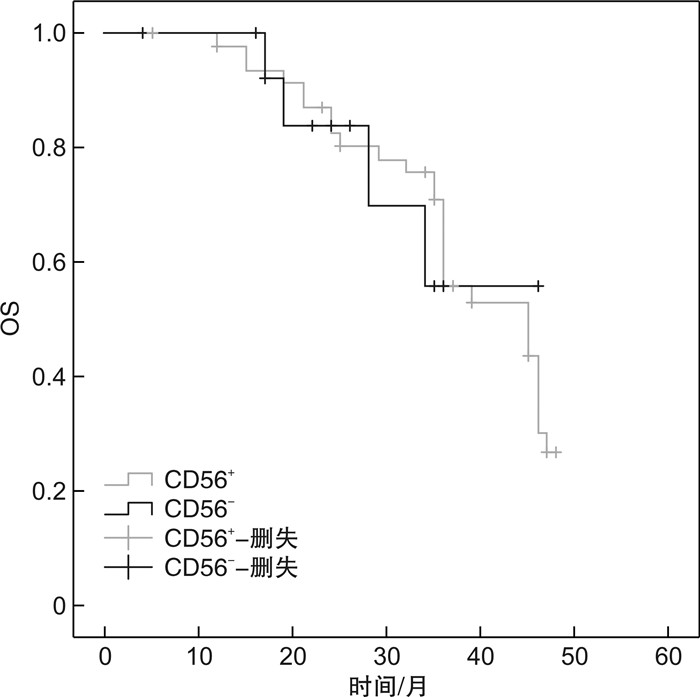
摘要: 分析初诊多发性骨髓瘤(MM)患者CD56表达差异与其预后的相关性,以硼替佐米联合来那度胺(VRd)为基础方案诱导治疗疗效的临床研究。回顾性分析山西医科大学第三医院血液科2015年1月—2021年8月初诊MM患者160例,分为CD56表达阳性组(CD56+)和CD56表达阴性组(CD56-),比较2组临床特征及总生存期(OS);其中以VRd方案诱导治疗4个疗程的初诊MM患者共64例患者,在4个疗程后进行疗效评估及OS的分析,比较2组疗效评估的差别。CD56+组109例(68.1%),CD56-组51例(31.9%);CD56-组β2微球蛋白(β2-MG)及乳酸脱氢酶水平(LDH)较CD56+组更高(P=0.04,P=0.03);CD56-组更易发生髓外病变(P < 0.01);CD56+组患者OS更长(P=0.04);CD56-、β2-MG≥8 mg/L是MM患者OS的独立预后不良因素(P < 0.05);经VRd方案治疗后,2组患者预后评估差异无统计学意义(P=0.60),中位OS差异无统计学意义(P=0.96);CD56-组β2-MG和LDH相对CD56+组下降更明显(P < 0.05)。由此可见,初诊CD56-MM患者具有更高的β2-MG和LDH,更易发生髓外侵袭,OS相对较短,经VRd方案诱导治疗的MM患者,2组疗效相当,进行OS分析差异无统计学意义,为CD56-患者更个体化的治疗提供帮助。Abstract: To analyze the correlation between CD56 expression difference and prognosis in newly diagnosed multiple myeloma(MM) patients, and to study the efficacy of bortezomib combined with lenalidomide based induction therapy(VRd). A retrospective analysis was performed on 160 cases of MM newly diagnosed in Third Hospital of Shanxi Medical University hematology department from January 2015 to August 2021, which were divided into CD56 positive group(CD56+) and CD56 negative group(CD56-). The clinical features and overall survival(OS) of the two groups were compared. Among them, a total of 64 newly diagnosed MM patients were treated with VRd for 4 courses. After 4 courses of treatment, efficacy evaluation and OS analysis were conducted. There are 109 cases(68.1%) in CD56+group and 51 cases(31.9%) in CD56-group. The levels of β2 microglobulin(β2-MG) and lactate dehydrogenase(LDH) in CD56-group were higher than those in CD56+group(P=0.04, P=0.03). Extramedullary lesions were more likely to occur in CD56-group(P < 0.01). The OS in CD56+group was longer than that in CD56-group(P=0.04). CD56-and β2-MG ≥8 mg/L were the independent adverse influencing factors of OS(P < 0.05). After treatment with VRd regimen, there was no difference in prognosis assessment and median OS between 2 groups(P=0.60). The decrease of β2-MG and LDH in CD56-group was more obvious than in CD56+group(P < 0.05). Above all, Newly diagnosed CD56-MM patients had higher β2-MG and LDH, were more prone to extramedullary invasion, and had a relatively short OS. For patients with MM treated with VRd regimen, the therapeutic efficacy of CD56+group and CD56-group was similar, and there was no significant difference in OS analysis, providing help for more individualized treatment of CD56-patients.
-
Key words:
- CD56 expression /
- multiple myeloma /
- bortezomib /
- lenalidomide
-
-
表 1 2组患者临床特征比较
临床特征 CD56+组(n=109) CD56-组(n=51) P 性别/例(%) 0.77 男 55(50.4) 27(52.9) 女 54(49.6) 24(47.1) 年龄/岁 63.3±10.3 65.20±11.3 0.90 血清钙水平/(mmol·L-1) 2.4±0.8 2.3±0.2 0.84 C反应蛋白/(mg·L-1) 5.5±2.8 8.9±2.7 0.42 血红蛋白/(g·L-1) 105.0±32.2 101.0±46.4 0.42 β2-MG/(mg·L-1) 8.2±3.4 18.5±4.7 0.04 LDH/(U·L-1) 185.0±32.0 269.0±51.5 0.03 白蛋白/(g·L-1) 36.1±3.9 34.2±5.2 0.62 Scr/(μmol·L-1) 121.0±57.2 153.0±42.5 0.31 免疫球蛋白亚型/例(%) 0.07 IgA 17(15.6) 17(33.3) IgE 11(10.1) 4(7.9) IgG 62(56.9) 25(49.0) 轻链型 19(17.4) 5(9.8) ISS分期/例(%) 0.17 Ⅰ、Ⅱ期 72(66.1) 28(54.9) Ⅲ期 37(33.9) 23(45.1) 髓外病变/例(%) < 0.01 有 15(13.8) 19(37.3) 无 94(86.2) 32(62.7) 表 2 MM患者的预后因素分析
预后因素 单因素分析 多因素分析 P HR 95%CI P CD56- 0.04 1.2 0.8~1.7 0.04 ISS分期Ⅲ期 0.02 2.6 1.0~5.3 0.06 LDH≥245 U/L 0.03 1.2 1.0~8.1 0.07 β2-MG≥8 mg/L 0.02 1.9 0.7~12.4 0.03 Scr≥176 μmol/L 0.14 表 3 2组MM患者治疗后疗效分析
例 组别 CR VGPR PR SD PD CD56+组 2 14 17 11 5 CD56-组 0 4 5 5 1 表 4 2组患者治疗后β2-MG、LDH变化
X±S 组别 时间 β2-MG/
(mg·L-1)LDH/
(U·L-1)CD56+组 治疗后 13.5±4.5 108.0±18.1 治疗前后差值 2.8±6.6 107.0±19.7 CD56-组 治疗后 20.2±6.7 46.7±41.6 治疗前后差值 14.0±13.9 191.0±77.1 P 0.01 0.03 -
[1] 中国医师协会血液科医师分会, 中华医学会血液学分会. 中国多发性骨髓瘤诊治指南(2020年修订)[J]. 中华内科杂志, 2020, 59(5): 341-346. https://www.cnki.com.cn/Article/CJFDTOTAL-JLYB201610002.htm
[2] Rajkumar SV, Kumar S. Multiple myeloma current treatment algorithms[J]. Blood Cancer J, 2020, 10(9): 94. https://www.nejm.org/doi/full/10.1056/NEJMe1407442
[3] 梅恒, 李成功, 胡豫. 嵌合抗原受体T细胞疗法在难治/复发多发性骨髓瘤中的研究进展[J]. 临床血液学杂志, 2020, 33(7): 441-445. https://www.cnki.com.cn/Article/CJFDTOTAL-LCXZ202007001.htm
[4] 王祥民, 徐开林. 多靶点CAR-T细胞治疗在复发难治性多发性骨髓瘤中的应用[J]. 临床血液学杂志, 2020, 33(7): 446-450. https://www.cnki.com.cn/Article/CJFDTOTAL-LCXZ202007002.htm
[5] Feng X, Zhang L, Acharya C, et al. Targeting CD38 Suppresses Induction and Function of T Regulatory Cells to Mitigate Immunosuppression in Multiple Myeloma[J]. Clin Cancer Res, 2017, 23(15): 4290-4300. doi: 10.1158/1078-0432.CCR-16-3192
[6] 吴桂香, 夏维林, 杨克, 等. 硼替佐米联合来那度胺及地塞米松治疗多发性骨髓瘤临床疗效观察[J]. 汕头大学医学院学报, 2020, 33(1): 31-33. https://www.cnki.com.cn/Article/CJFDTOTAL-STDY202001009.htm
[7] 孙欢, 杜燕, 徐陆忠, 等. CD56、CD117表达水平与来那度胺治疗多发性骨髓瘤疗效的相关性分析[J]. 现代生物医学进展, 2020, 20(1): 72-75. https://www.cnki.com.cn/Article/CJFDTOTAL-SWCX202001016.htm
[8] 梁艳, 伦伟丹, 刘礼平. CD56在多发性骨髓瘤诊断及分型中的临床应用[J]. 当代医学, 2019, 25(17): 83-85. https://www.cnki.com.cn/Article/CJFDTOTAL-DDYI201917033.htm
[9] Skerget M, Skopec B, Zadnik V, et al. CD56 Expression Is an Important Prognostic Factor in Multiple Myeloma Even with Bortezomib Induction[J]. Acta Haematol, 2018, 139(4): 228-234.
[10] Van Camp B, Durie BG, Spier C, et al. Plasma cells in multiple myeloma express a natural killer cell-associated antigen: CD56(NKH-1;Leu-19)[J]. Blood, 1990, 76(2): 377-382.
[11] Harrington A, Hari P, Kroft S. Utility of CD56 immunohis-tochemical studies in follow-up of plasma cell myeloma[J]. Am J Clin Pathol, 2009, 132(1): 60-66. https://academic.oup.com/ajcp/article/132/1/60/1766014
[12] 张彩霞. CD56在多发性骨髓瘤中的研究进展[J]. 疑难病杂志, 2020, 19(7): 747-749. https://www.cnki.com.cn/Article/CJFDTOTAL-YNBZ202007029.htm
[13] Koumpis E, Tassi I, Malea T, et al. CD56 expression in multiple myeloma: Correlation with poor prognostic markers but no effect on outcome[J]. Pathol Res Pract, 2021, 225: 153567.
[14] 王静, 张丽娜, 史青林, 等. 伴髓外病变的初诊多发性骨髓瘤患者临床特征及预后分析[J]. 中华血液学杂志, 2020, 41(10): 822-828. https://www.cnki.com.cn/Article/CJFDTOTAL-TJYZ202005013.htm
[15] 李高, 黄秀娟, 牛彤, 等. 多发性骨髓瘤肿瘤细胞CD56表达与髓外病变和髓外复发的关系[J]. 中国实验血液学杂志, 2021, 29(2): 553-556. https://www.cnki.com.cn/Article/CJFDTOTAL-XYSY202102044.htm
[16] Okura M, Ida N, Yamauchi T. The clinical significance of CD49e and CD56 for multiple myeloma in the novel agents era[J]. Med Oncol, 2020, 37(11): 103.
[17] Zhang L, Huang Y, Lin Y, et al. Prognostic significance of CD56 expression in patients with multiple myeloma: a meta-analysis[J]. Hematology, 2022, 27(1): 122-131. https://link.springer.com/article/10.1007/s12032-011-0104-9
[18] Ceran F, Falay M, Daǧdaş S, et al. The Assessment of CD56 and CD117 Expressions at the Time of the Diagnosis in Multiple Myeloma Patients[J]. Turk J Haematol, 2017, 34(3): 226-232.
[19] 路瑾, 黄晓军. 来那度胺在血液恶性肿瘤中的应用[J]. 中华内科杂志, 2013, 52(9): 777-780.
[20] Jagannath S, Richardson PG, Sonneveld P, et al. Bortezomib appears to overcome the poor prognosis conferred by chromosome 13 deletion in phase 2 and 3 trials[J]. Leukemia, 2007, 21(1): 151-157.
-
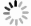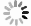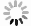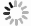



 下载:
下载: